뉴스룸뇌졸중 뉴스
- Safety and efficacy of platelet glycoprotein VI inhibition in acute ischaemic stroke (ACTIMIS): a randomised, doubleblind, placebo-controlled, phase 1b/2a trial
-
- 관리자
- 2024-02-29
- 조회수 : 250
Link URL : https://
Safety and efficacy of platelet glycoprotein VI inhibition in acute ischaemic stroke (ACTIMIS): a randomised, doubleblind, placebo-controlled, phase 1b/2a trial
Mazighi M, et al. Lancet Neurol. 2024, 10.1016/S1474-4422(23)00427-1
Introduction
재관류 치료와 함께 사용하는 glycoprotein VI-triggered platelet activation 길항제는 급성 허혈성 뇌졸중에서 유망한 치료약제이다. Glenzocimab은 혈소판 당단백질 VI의 작용을 억제하는 항체의 일부이다. 지난 Phase I 연구에서 건강한 대상자를 대상으로 출혈 발생 등의 부작용 등, 안전성을 입증하였다.
Objectives
기계적 혈전 제거술 시행 유무에 관계없이 alteplase 치료를 받을 수 있는 급성 허혈성 뇌졸중 환자에서 Glenzocimab의 최적 용량의 안전성과 효능을 확인하고자 하였다.
Methods
● 유럽 6개국, 26개 뇌졸중센터에서 시행한 무작위 이중 눈가림 대조군 연구
● 대상자: 만 18세 이상, 허혈성 뇌졸중환자, alteplase 투여 전 NIHSS≥6
● 치료
- 정맥 투여 종료 시 총 투여 용량:
1b: Glenzocimab 또는 위약 125mg, 250mg, 500mg, 1000mg,
2a: Glenzocimab 또는 위약 1000mg
- alteplase 치료를 받은 환자 중, 뇌졸중 증상 발현 4~5시간 이내에 투여 시작
● 1차 평가변수
- 안전성, 사망률, 두개내출혈
● 2차 유효성 평가변수
- 혈전 용해술 전부터 24시간까지의 NIHSS 점수의 변화, 90일째의 mRS 점수측정를 통한 신경학적 회복, 재관류(혈관 조영술을 사용하여 기계적 혈전 제거술을 받은 환자에서만 평가, mTICI)
● 통계분석: All-cause mortality in phase 2a with the Kaplan-Meier method, and survival curves between treatment groups with the log-rank test, efficacy outcomes in phase 2a with both descriptive and model-based approaches (ANCOVA tests and 95% CIs)
Results
● 2019년 3월 6일부터 2021년 6월 27일까지 모집된 환자 60명을 무작위로 Glenzocimab 125mg, 250mg, 500mg, 1000mg 또는 위약에 배정하여 1b(그룹당 n=12), 안전성 분석에 배정했다.
● 2020년 10월 2일부터 2021년 6월 27일까지 106명의 환자를 무작위로 Glenzocimab 1000mg(n=53) 또는 위약(n=53)에 배정했다.
● 가장 빈번하게 발생한 이상 반응은 비증상성 출혈 변환이었다. Glenzocimab 치료를 받은 환자 54명 중 17명(31%)과 위약 치료를 받은 환자 52명 중 26명(50%)에서 발생하였다(Table2).
● 카플란-마이어 생존 확률은 그룹 간에 차이가 있었다(hazard ratio 0.29 [95% CI 0.09-0.90], log-rank p=0.035; figure 2).
● 초기에서 24시간까지의 NIHSS 점수 변화는 글렌조시맙 1000mg과 위약 간에 차이가 없었다. 초기 평가 대비 절대중앙값의 변화, -3.0 (IQR -7.0~0.0), -3.5 (-9.0~0.5)
● 90일째 mRS 점수는 그룹 간에 통계적으로 유의미한 차이가 없었다(p=0.88; figure 3).
Conclusions
Glenzocimab 1000mg과 alteplase 병용 요법은 기계적 혈전 제거술의 유무에 관계없이 내약성이 우수했으며, 심각한 이상 반응, 두개 내 출혈, 사망률을 감소시킬 수 있다.

Table2: Adverse events (safety population)

Figure 2: Kaplan-Meier curves for all-cause mortality at day 90 (phase 2a), post-hoc analysis
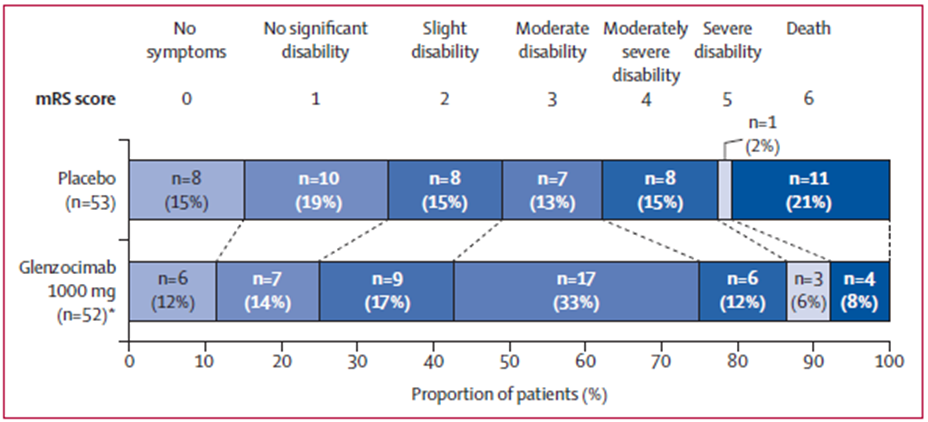
Figure 3: mRS scores at 3 months by study treatment group (phase 2a)

 HOME
HOME LOGIN
LOGIN
